
糖尿病血管合併症や薬の副作用のリスクに男女差はあるのか?
疾患の状態は一人ひとりで千差万別であり、同じ病気であっても同じ治療を行うことは、必ずしも正しくない場合がある。一人ひとりにあった医療、すなわち個別化医療の実現は、より良い医療のために必須であり、医療に携わる者全体の課題と言える。
近年、男女の差を念頭に置いて行う医療(いわゆる、性差医療)は、この個別化医療の実現や疾患の予防・改善に大きく貢献するとされ、欧米ではその重要性が広く知られている1。しかし現状では、ほとんどの疾患に性差が存在すると考えられているものの、その実態や原因には不明な点が多い2。また、男性と女性では、体格などの生物学的な特徴や、薬が身体の中でどう動くか(表1)、薬の作用の仕方(表2)などに明らかな違いがあるものの3-5、生殖器疾患や骨粗鬆症などの一部の疾患を除いて、薬物治療に性差を考慮することは十分に行われていない。
表1. 薬物動態の性差3,5 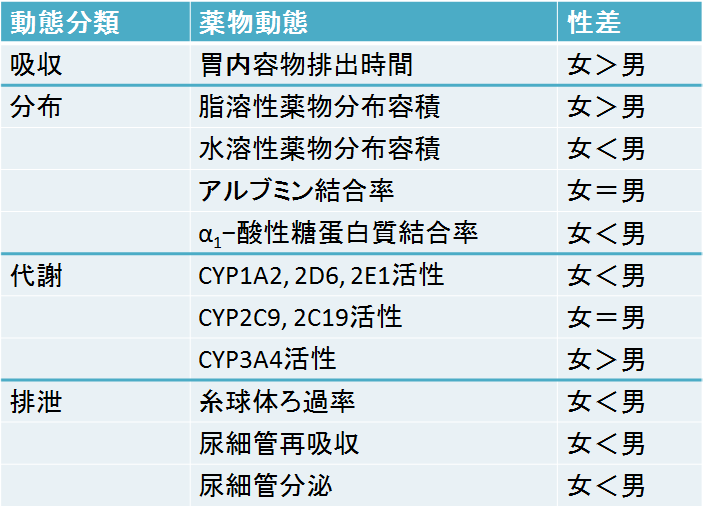
表2. 薬力学の性差により女性に多い有害反応3,4 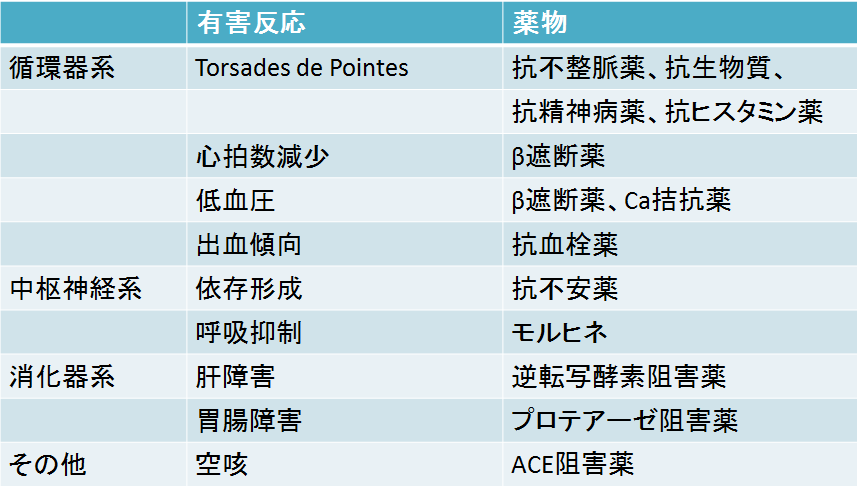
そこで我々は、①罹患率が高く (平成24年度の日本において、糖尿病が強く疑われる者と糖尿病の可能性を否定できない者との合計は2050万人6)、健康や医療経済に重大な影響を及ぼす糖尿病の血管合併症の性差に注目し、女性の2型糖尿病患者は男性に比べて糖尿病網膜症7,8及び腎機能障害のリスクが高いことを明らかにした(2型糖尿病患者を対象とした糖尿病血管合併症における性差の検討)。さらに、②熊本県薬剤師会と共同で、日本薬剤師会Drug Event Monitoring (DEM) 事業のデータを再解析し、糖尿病治療薬9,10、高血圧治療薬11、睡眠薬12及び気管支喘息治療薬13使用中の副作用発現のリスクに性差があることを明らかにした (熊本県薬剤師会DEM事業データを用いた副作用発現における性差の検討)。
現在、医療現場で用いられている治療ガイドライン (治療を行う際の一般的な基準) の多くは、男性で得られた情報に基づいて作成されている。これには、女性には性周期 (月経)があるために基礎実験や臨床試験の方法が複雑になりやすいことや、妊娠する可能性がある女性は、母体や胎児への影響の恐れから臨床試験に参加しにくいことなどが原因となっている2,14。しかしながら、そのような男性メインの情報に基づいた医療では、女性ではフィットせず、不利益を被る可能性も高いと考えられる(図1)。疾患の発症・進展や治療効果・副作用発現に関係する性差は多岐に渡り、生物学的性差のみならず、社会的役割や認知・行動などの心理社会的性差にも考慮した包括的介入が重要となる15,16(図2)。性差医療の歴史はまだ浅いが、臨床と基礎研究の双方からのアプローチにより性差に関する情報が蓄積することは、男女間格差の解消や個別化医療の実現に大きく寄与すると考えられる。同時に、性差の情報は積極的に臨床還元されるべきであり、特に医療従事者への性差医療の概念・意識の定着が望まれる。
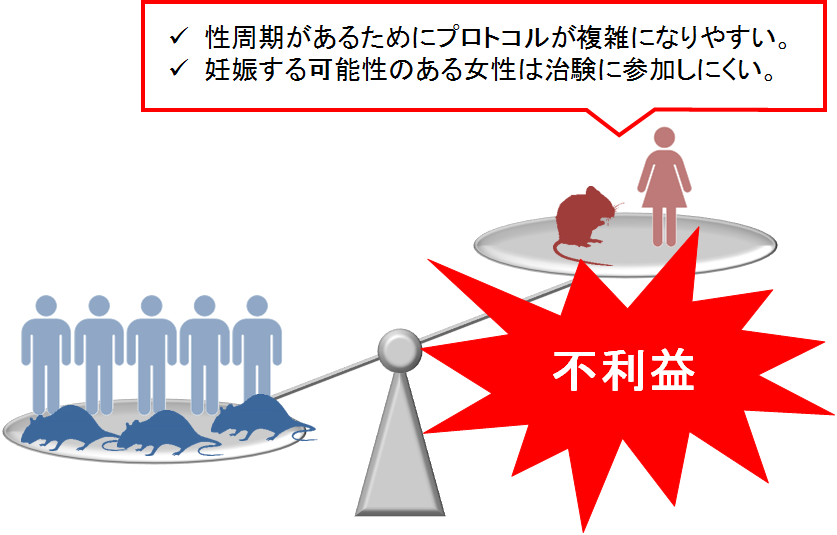
図1. 男性メインのデータによる治療ガイドライン2,14
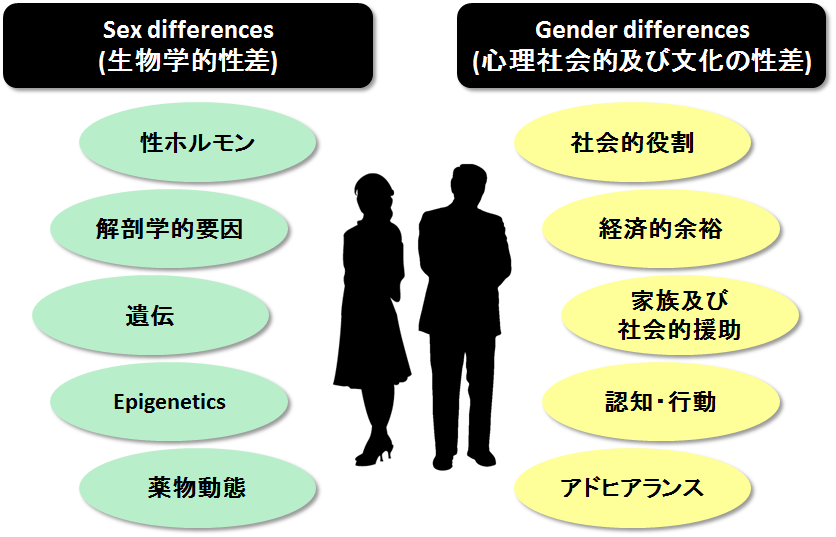
図2. 性差を考慮した治療選択15,16
1-1. 糖尿病網膜症の発症における性差7
糖尿病専門病院で半年以上治療を受けた2型糖尿病患者383人 (男性 245人、女性138人;平均年齢59.4歳;糖尿病罹病期間11.0年;観察期間5.8年) を対象に、糖尿病網膜症発症頻度を計算すると、1年間に1000人当たり、男性では36.0人、女性では54.5人であった(図3)。女性は男性に比べて糖尿病網膜症の発症リスク(網膜症になりやすさ)が1.9倍高いことが示された(図3)。
この要因として、女性の糖尿病診断の遅れと高血糖関連の血管障害が女性で起きやすいことが考えられた。
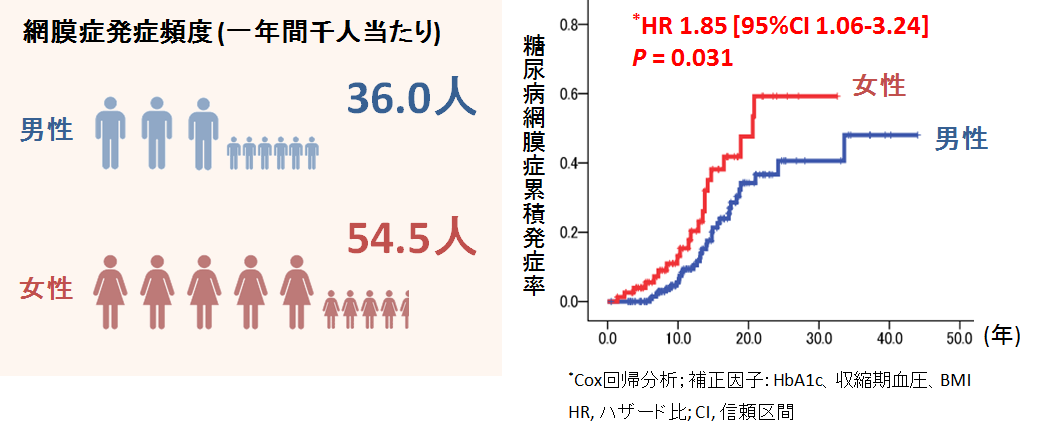
図3. 糖尿病網膜症発症リスクの性差7
1-2. Cytochrome P450 2C19遺伝子多型が糖尿病網膜症リスクに及ぼす影響における性差8
Cytochrome P450 2C19 (CYP2C19) は、肝臓で多くの薬を排泄しやすい形に変える働きを持つことで知られるが、血管内皮では血管保護作用を持つと考えられている(図4)。一方で、CYP2C19の働きの強さは遺伝的に個人差が大きく、日本人の約20%がこのCYP2C19の活性を消失(欠損)していることが知られている。
1-1と同じ集団において、CYP2C19遺伝子多型が糖尿病網膜症リスクに及ぼす影響を男女別に検討したところ、女性でのみCYP2C19遺伝子多型の影響が認められた。女性のCYP2C19の欠損者は非欠損者に比べて、糖尿病網膜症リスクが4.2倍であった(図5)。
CYP2C19の代謝生成物であるEETsはエストロゲンにより生成が促進され、女性にとって特に重要な血管保護因子である。女性の糖尿病患者では、CYP2C19遺伝的欠損によるEETs発現量低下が、血管保護作用の低下に影響して、糖尿病網膜症のリスクに関係したと考えられた。

図4. CYP2C19と血管障害17-19
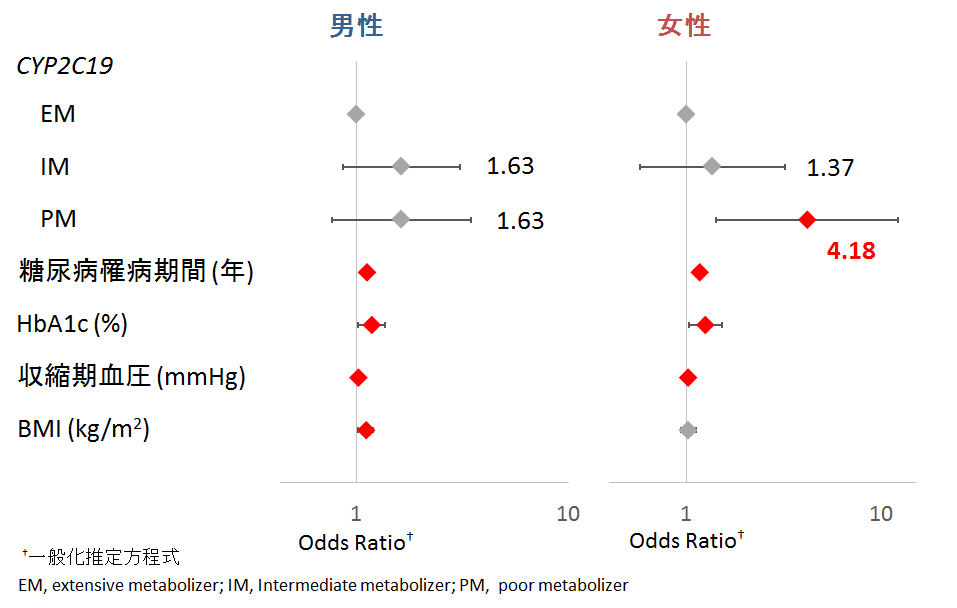
図5. CYP2C19遺伝子多型と網膜症リスク8
1-3. 腎機能障害における性差
現在論文投稿中
日本薬剤師会DEM事業は、薬局が医薬品の適正使用に一層貢献することを目的として、2002年から年に1回実施されている副作用調査である 。本検討では、熊本大学薬学部附属育薬フロンティアセンターと熊本県下700件の保険薬局との情報ネットワーク (KUMAYAKU Network for Community Pharmacies) により、熊本県独自に収集された2004-11年の延べ3万人に対する副作用聞き取り調査結果を、性差の観点から詳細に再解析した。
主な結果を表3に示す。調査対象医薬品は頻用医薬品であり、性差の検討を目的として選択されたものではないにも関わらず、8系統のうち5系統の薬剤 [糖尿病治療薬のsulfonylurea (SU) 剤及びdipeptidyl peptidase-4 (DPP-4) 阻害薬、高血圧治療薬のジヒドロピリジン系カルシウム拮抗薬、長短時間睡眠導入剤のゾルピデム、気管支喘息治療薬の吸入ステロイド] で女性の副作用発現率が高かった。これらの機序としては、年齢や性ホルモン、解剖学的・生物学的性差、飲酒の影響の性差などが複雑に関与していると推察された。従って、これらの薬を用いる際には、特に女性での副作用発現に注意すべきであり、性差を考慮した治療介入 (糖尿病治療薬や睡眠薬服用時の節酒、吸入ステロイド使用時のうがいの徹底など) が重要と考えられた。
表3. 副作用発現における性差9-13 ←画像クリックで元の大きさで表示
←画像クリックで元の大きさで表示
References
1. National Institutes of Health Office of Research on Women's Health. Moving into the future with new dimensions and strategies : a vision for 2020 for women's health research. (2010)
2. Shimokawa, H. [The history and perspective of gender-specific medicine in Japan]. Nihon Rinsho 73, 547-550 (2015).
3. Franconi, F., Brunelleschi, S., Steardo, L. & Cuomo, V. Gender differences in drug responses. Pharmacol Res 55, 81-95 (2007).
4. Ofotokun, I. Sex differences in the pharmacologic effects of antiretroviral drugs: potential roles of drug transporters and phase 1 and 2 metabolizing enzymes. Top HIV Med 13, 79-83 (2005).
5. Sato, H.U., K. [Sex differences in pharmacokinetics and pharmacodynamics]. Nihon Rinsho 73, 542-546 (2015).
6. 厚生労働省. 平成24年 国民健康・栄養調査.
http://www.mhlw.go.jp/file/04-Houdouhappyou-10904750-Kenkoukyoku-Gantaisakukenkouzoushinka/0000099296.pdf (2013).
7. Kajiwara, A., et al. Gender differences in the incidence and progression of diabetic retinopathy among Japanese patients with type 2 diabetes mellitus: a clinic-based retrospective longitudinal study. Diabetes Res Clin Pract 103, e7-10 (2014).
8. Kajiwara, A., et al. Sex differences in the effect of cytochrome P450 2C19 polymorphisms on the risk of diabetic retinopathy: a retrospective longitudinal study in Japanese patients with type 2 diabetes. Pharmacogenet Genomics 23, 717-720 (2013).
9. Kajiwara, A., et al. Higher risk of sulfonylurea-associated hypoglycemic symptoms in women with type 2 diabetes mellitus. Clin Drug Investig 35, 593-600 (2015).
10. Kajiwara, A., et al. Risk Factors for Adverse Symptoms During Dipeptidyl Peptidase-IV Inhibitor Therapy: A Questionnaire-Based Study Carried Out by the Japan Pharmaceutical Association Drug Event Monitoring Project in Kumamoto Prefecture. Drug Saf 36, 981-987 (2013).
11. Kajiwara, A., et al. Younger females are at greater risk of vasodilation-related adverse symptoms caused by dihydropyridine calcium channel blockers: results of a study of 11,918 Japanese patients. Clin Drug Investig 34, 431-435 (2014).
12. Kajiwara, A., et al. Safety analysis of zolpidem in elderly subjects 80 years of age or older: adverse event monitoring in Japanese subjects. Aging Ment Health, 1-5 (2015).
13. Kajiwara, A., et al. Absence of gargling affects topical adverse symptoms caused by inhaled corticosteroids in females. J Asthma 51, 221-224 (2014).
14. Mauvais-Jarvis, F. Elucidating sex and gender differences in diabetes: a necessary step toward personalized medicine. J Diabetes Complications 29, 162-163 (2015).
15. Amano, K. [Gender difference in the mortality and prevalence in Japan]. Nihon Rinsho 73, 551-556 (2015).
16. Franconi, F., Campesi, I., Occhioni, S. & Tonolo, G. Sex-gender differences in diabetes vascular complications and treatment. Endocr Metab Immune Disord Drug Targets 12, 179-196 (2012).
17. Fer, M., et al. Cytochromes P450 from family 4 are the main omega hydroxylating enzymes in humans: CYP4F3B is the prominent player in PUFA metabolism. J Lipid Res 49, 2379-2389 (2008).
18. Wang, Z., Yadav, A.S., Leskova, W. & Harris, N.R. Inhibition of 20-HETE attenuates diabetes-induced decreases in retinal hemodynamics. Exp Eye Res 93, 108-113 (2011).
19. Zordoky, B.N. & El-Kadi, A.O. Effect of cytochrome P450 polymorphism on arachidonic acid metabolism and their impact on cardiovascular diseases. Pharmacol Ther 125, 446-463 (2010).


















